Le Cabinet Médical Nation recherche, en vue d'une installation :
Utilisation du misoprostol (Cytotec ®, Gymiso ®) hors AMM en gynécologie-obstétrique
- Affichages : 89516
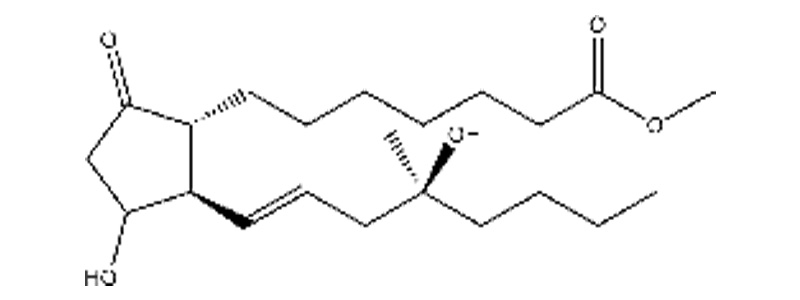 Généralités
Généralités
Le misoprostol est un médicament de la famille des prostaglandines. C’est une prostaglandine de synthèse, analogue aux PGE1 naturelles.
En France, chaque médicament fabriqué industriellement, avant d’être commercialisé, doit faire l’objet d’une autorisation de mise sur le marché (AMM).
Cette autorisation est délivrée par les autorités compétentes européennes ou nationales que sont la Commission européenne, après avis de l’agence européenne d’évaluation des médicaments (EMA), ou l’ANSM (Agence Nationale de Sécurité du Médicament et des produits de santé).
Le misoprostol (Cytotec ®, Gymiso ®) fait partie de ces médicaments, très largement prescrits en gynécologie-obstétrique, hors AMM.
La société Pfizer à décidé de mettre fin à la commercialisation de la spécialité Cytotec à compter du 1er mars 2018.
Prescriptions hors AMM
Si le praticien bénéficie en principe d'une totale liberté de prescription, celle-ci trouve sa limite dans l'obligation qui lui est faite de ne pas faire courir de risques à ses patients, ou encore dans l'interdiction posée par l'article R 4127-39 CSP qui énonce que « Les médecins ne peuvent proposer aux malades ou à leur entourage comme salutaire ou sans danger un remède ou un procédé illusoire ou insuffisamment éprouvé ».
Parce qu'elle s'inscrit hors du cadre autorisé, une prescription hors AMM peut paraître par principe suspecte. A défaut de texte encadrant cette pratique, celle-ci était jusqu'à présent laissée à l'appréciation des magistrats.
La loi n° 2011-2012 du 29 décembre 2011 relative au renforcement de la sécurité sanitaire du médicament et des produits de santé a été publiée au journal officiel du 30 décembre 2011.
Il ressort de cette jurisprudence, qu'une prescription hors AMM n'est pas de facto considérée comme illégale et nécessairement fautive.
En effet, le Conseil d'Etat et la Cour de cassation ont tous deux admis à plusieurs reprises et encore récemment, avant l'entrée en vigueur de la loi de 2011, que le médecin pouvait établir une prescription hors AMM, dès lors que :
- Le traitement est reconnu comme efficace et non dangereux par la communauté et la littérature scientifiques,
- Le médecin est en mesure de justifier son indication et son geste au regard de l'état du patient, de sa demande et des connaissances scientifiques du moment.
La nouvelle loi ne revient pas sur cette interprétation. Au contraire, par l'insertion d'un article L 5121-12-1 au sein du code de la santé publique, elle confère à cette pratique une assise légale tout en en encadrant les contours dans un souci de protection des patients. Ce texte énonce explicitement « Une spécialité pharmaceutique peut faire l'objet d'une prescription non conforme à son autorisation de mise sur le marché ».
Mécanisme d’action
Le misoprostol a une action anti-sécrétoire gastrique. Il provoque également des contractions des fibres musculaires lisses du myomètre et un relâchement du col utérin.
Indications générales avec AMM
- Traitement de l'ulcère gastrique ou duodénal évolutif ;
- Traitement des lésions gastroduodénales induites par les AINS, en se limitant aux sujets chez qui la poursuite des anti-inflammatoires est indispensable ;
- Traitement préventif des lésions gastriques et duodénales et des complications gastroduodénales graves induites par les AINS chez les sujets à risque (notamment, âge > 65 ans, antécédents d'ulcère gastroduodénal ou d'intolérance aux AINS) pour lesquels un traitement anti-inflammatoire est indispensable.
Indications en gynécologie-obstétrique avec AMM
Le Gymiso ® est la spécialité de misoprostol qui a l’AMM en gynécologie-obstétrique. Il est dosé à 200 microgrammes par comprimé.
- Interruption médicale de grossesse intra-utérine, en association à la mifépristone (Mifégyne ®), au plus tard au 49ème jour d'aménorrhée. La posologie de Gymiso® est de 400 microgrammes, soit 2 comprimés en une prise par voie orale 36 à 48 heures après la prise orale de mifépristone (Mifégyne ®) .
- Préparation du col utérin avant interruption chirurgicale de grossesse au cours du premier trimestre. La posologie de Gymiso ® est de 400 microgrammes, soit 2 comprimés en une prise par voie orale 3 à 4 heures avant l'intervention chirurgicale.
Indications en gynécologie-obstétrique hors AMM
Premier trimestre de la grossesse
Dilatation du col avant geste chirurgical (aspiration)
Dans cette indication, l’utilisation de misoprostol permet de faciliter la dilatation cervicale, de diminuer la durée de l’intervention et de réduire le risque de rétention utérine secondaire.
L’administration du misoprostol par voie vaginale à la dose de 400 microgrammes 3 heures avant l’intervention est plus efficace que par voie orale.
Grossesse arrêtée
L’utilisation de misoprostol pour l’évacuation d’une grossesse arrêtée représente une alternative thérapeutique au traitement chirurgical ou à l’expectative. Elle permet la plupart du temps d’éviter une anesthésie générale et une hospitalisation. Cette alternative est tout de même responsable de saignements plus prolongés et de douleurs plus fréquentes que le traitement chirurgical.
Dans cette indication, après confirmation de l’arrêt de la grossesse, comme pour les interruptions volontaires de grossesse, le misoprostol est habituellement utilisé au plus tard au 49ème jour d'aménorrhée (soit un embryon arrêté dont la longueur mesure 10 mm au maximum).
Le meilleur protocole est l’administration de 800 microgrammes de misoprostol, soit 4 comprimés en une prise par voie vaginale, éventuellement renouvelée 24 à 48 heures plus tard. L’efficacité est alors supérieure à 80 %.
Fausse couche spontanée incomplète
Le misoprostol n’apporte pas de bénéfice par rapport à l’expectative au à l’aspiration chirurgicale en cas de fausse couche spontanée incomplète.
Interruption médicale de grossesse
En cas d’interruption médicale de grossesse, entre 7 SA et 14 SA : seule la technique médicale permet un examen foetopathologique correct.
Le protocole thérapeutique consiste à l’administration de mifépristone (Mifégyne ®) 200 mg par voie orale, suivie 24 à 48h plus tard d’une prise de 800 microgrammes de misoprostol par voie vaginale ou orale, éventuellement complétée d’une dose de 400 microgrammes 3 à 4h plus tard.
Deuxième et troisième trimestres de la grossesse
Interruption médicale de grossesse et mort in utero
Au deuxième trimestre de la grossesse, l’utilisation de la de la mifépristone (Mifégyne ®) avec une posologie d’au moins 200 mg voire 600 mg, suivie 36 à 48h plus tard de misoprostol par voie intra vaginale à la dose de 800 à 2 400 microgrammes/24 h en prises espacées de 3 à 6h est une alternative aux autre thérapeutiques qui comportent plus de risques.
Entre 28 et 37 SA aucune prostaglandine n’a l’AMM pour l’interruption médicale de grossesse. L’utilisation du misoprostol dans les mêmes conditions qu’au deuxième trimestre est possible.
Maturation cervicale au troisième trimestre
L’utilisation de misoprostol par voie vaginale à la dose de 25 microgrammes (1/8ème de comprimé) toutes les 3 à 6h sur un col défavorable est une alternative pour la maturation cervicale à terme sur fœtus vivant.
Hémorragie du post-partum
L’utilisation de misoprostol à une dose de 800 microgrammes par voie sublinguale en cas d’hémorragie du post-partum par atonie utérine après la naissance de l’enfant est possible SEULEMENT en cas de non disponibilité de l’ocytocine.
Utilisation en gynécologie pour la dilatation du col
Avant hystéroscopie
Le recours à ce traitement présente un bénéfice avant la réalisation d’une hystéroscopie diagnostique ou une hystéroscopie opératoire chez les patientes non ménopausées. Il devrait être réservé aux cas supposés difficiles du fait de ses effets secondaires.
Avant la pose d’un dispositif intra-utérin (stérilet)
Il n’apporte aucun bénéfice dans cette indication.
Contre-indications
- Hypersensibilité à la substance active, à l'un des excipients ou à d'autres prostaglandines ;
- Femme en âge de procréer, en l'absence de contraception efficace ;
- Femme enceinte, ou dont la grossesse n'est pas exclue ou envisageant une grossesse, le misoprostol ayant une puissante activité sur la contractilité du muscle utérin, et pouvant entraîner une interruption de grossesse.
Effets secondaires
- Réaction anaphylactique ;
- Sensation vertigineuse, céphalées ;
- Diarrhée ;
- Douleurs abdominales, constipation, flatulences, dyspepsie, nausées, vomissements ;
- Rash ;
- Spasmes coronaires, infarctus du myocarde, accident vasculaire cérébral ;
- Fièvre ;
- Frissons.
Effets secondaires en gynécologie-obstétrique
- Embolie amniotique, contractions utérines anormales, mort foetale, avortement incomplet, naissance prématurée, rétention placentaire, rupture utérine, perforation utérine ;
- Hémorragie vaginale (dont saignement vaginal postménopausique), saignements intermenstruels, troubles menstruels et spasme utérin ;
- Ménorragie, dysménorrhée ;
- Hémorragie utérine ;
- Malformations congénitales.
Exposition in utero
Le risque tératogène d’une exposition au premier trimestre de la grossesse augmente le risque global de malformations congénitales d’un facteur 3,9.
Il existe par ailleurs un risque malformatif spécifique d’environ 4% en cas d’exposition au premier trimestre de la grossesse : syndrome de Möbius, associant des anomalies craniofaciales (paralysie des 6e et 7e, voire 5e nerfs crâniens, entraînant une hypomimie, des anomalies de la succion, de la déglutition et des mouvements oculaires, hydrocéphalies) et des membres (anomalies réductionnelles, arthrogrypose, pieds bots...).
Il est possible d’autoriser la poursuite de la grossesse chez une patiente exposée au premier trimestre de la grossesse au misoprostol, mais alors, avec un suivi par échographie morphologique orientée sur le massif facial, sur les membres et sur le système nerveux central. Cette échographie doit être pratiquée par un échographiste spécialisé au diagnostic anténatal.
RTU (recommandation temporaire d’utilisation) du misoprostol
Le 30 janvier 2018 il a été décidé de la création d'un comité scientifique spécialisé temporaire « RTU - MISOPROSTOL » à l'Agence nationale de sécurité du médicament et des produits de santé dont l'objectif sera de donner un avis sur l'élaboration de recommandations temporaires d'utilisation du misoprostol dans les indications suivantes :
- lnterruption médicale de grossesse ;
- Mort fætale in utero ;
- Fausse couche spontanée.
Ce comité scientifique a été désigné pour une durée de un an.
Quelles alternatives au Cytotec ?
Il existe deux médicaments contenant du misoprostol. Le Gymiso ® du laboratoire Amring et le MisoOne ® de Nordic Pharma. Mais leur utilisation de mise sur le marché (AMM) ne concerne que les IVG médicamenteuses. L’ANSM leur a alors accordé une recommandation temporaire d’utilisation pour les déclenchements de l'accouchement et les fausses-couches, effective, normalement, au 1er mars prochain. Un troisième médicament a reçu une autorisation de mise sur le marché (AMM) : le danois Angusta ® du laboratoire Azanta. Mais il ne sera pas disponible en France avant plusieurs mois.
Sources
CNGOF 2013
Vidal : http://www.vidal.fr/substances/2398/misoprostol/